 中文
中文
僅僅一年前,安娜·布拉克尼(Anna Blakney)還在倫敦實驗室從事不太引人注目的小領域科學研究。在她科學界之外的朋友中,很少有人聽說過mRNA疫苗。因為當時這類疫苗還不存在。在她2019年發表的年度會議演講中,與會者可能只有幾十人。
如今,她備受追捧:她是加拿大英屬哥倫比亞大學(University of British Columbia)的助理教授,也是一名科學傳播者,在TikTok上有25.3萬名粉絲和370萬個讚。她承認,她在正確的時間、正確的地點趕上了一代人一次的科學進步浪潮。她甚至給這個新時代起了個名字:「RNA復興」(RNAissance)。
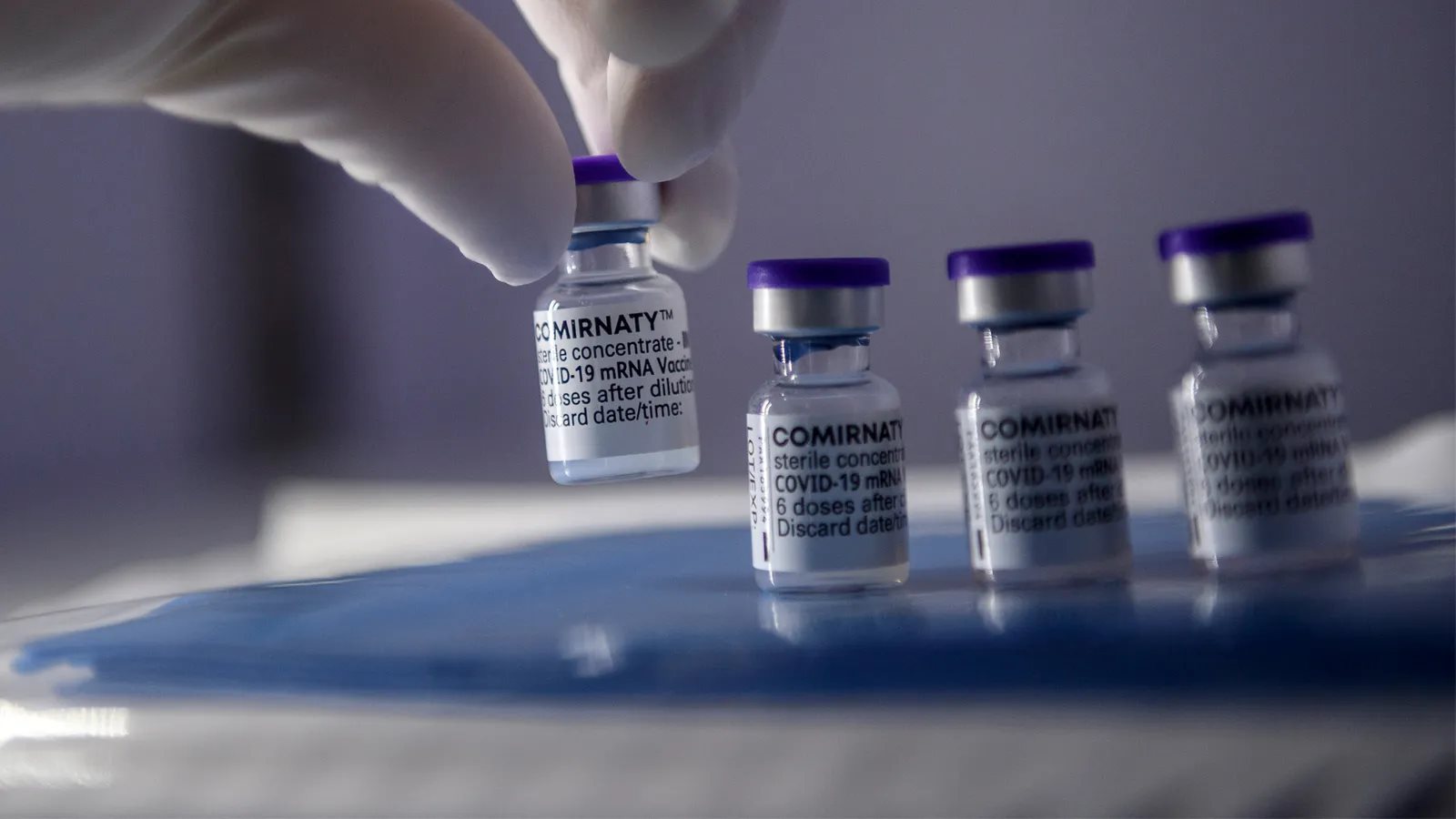
由於新冠病毒大流行,許多人已經聽說並接受了來自輝瑞生物科技(Pfizer-BioNTech)和莫德納(Moderna)等公司的mRNA疫苗。但即便是2016年,布萊克尼在倫敦帝國理工學院(Imperial College London)開始攻讀博士學位時,「很多人都懷疑這種方法是否可行」。現在,「整個mRNA領域正在爆棚。它改變了醫學界的遊戲規則。」
這是巨大改變,它提出了非常宏大的、令人興奮的問題:mRNA疫苗能治療癌症、艾滋病、熱帶疾病,甚至給與我們超人的免疫力嗎?
信使核糖核酸,簡稱mRNA,是一種單鏈分子,它攜帶從DNA到細胞蛋白質製造機制的遺傳密碼。沒有mRMA,人類的遺傳密碼就不能被使用,蛋白質就不能被製造,身體就不能工作。如果說DNA是銀行卡,那麼mRNA就是讀卡器。

一旦病毒進入細胞,就會釋放自己的RNA,誘使被劫持的細胞以病毒蛋白質的形式吐出病毒副本,從而破壞免疫系統。傳統疫苗的工作原理是,注射被稱為抗原的滅活病毒蛋白質,當病毒再次出現,抗原會刺激人體免疫系統識別病毒。mRNA疫苗的絶妙之處在於它不需要注射抗原本身。這些疫苗使用的是將抗原的基因序列或「代碼」翻譯成的mRNA。它如同真實存在的鬼魂,欺騙身體產生真實的抗體。然後,人工mRNA本身消失,被人體的自然防禦機制(包括分解它的酵素)降解,留給我們的只有抗體。
因此,與傳統疫苗相比,mRNA疫苗的生產更安全、更快、更便宜。你不再需要巨大的生物安全實驗室,在數百萬個雞蛋中培育致命病毒。只需一個實驗室就可以對抗原的蛋白質進行測序,並將其通過電子郵件發送到世界各地。有了這些信息,實驗室可以「在一個100毫升的試管中製造出100萬劑量的mRNA,」布萊克尼說。
我們現在已經看到了這個過程如何實時運行。2020年1月10日,中國疾病預防控制中心人畜共患疾病專家張永振對新冠病毒基因組進行測序,並於次日發佈。世界衛生組織於3月11日宣佈2019冠狀病毒病為全球大流行病。3月16日,利用張永振提供的序列,首個mRNA疫苗開始了一期臨牀試驗。美國食品和藥物管理局(Food and Drug Administration)於2020年12月11日批准了輝瑞生物科技公司研發的新型冠狀病毒疫苗,不僅成為首個獲批用於人類的mRNA疫苗,而且是首個在臨牀試驗中有效率達到95%的疫苗。12月18日,莫德納的mRNA疫苗緊隨其後獲得批准。此前,腮腺炎疫苗花了四年時間才成為「有史以來最快的疫苗」,而莫德納和輝瑞的疫苗只用了11個月。
mRNA疫苗背後的理論由賓夕法尼亞大學(University of Pennsylvania)的科學家卡塔林·卡里科(Katalin Karikó)和德魯·韋斯曼(Drew Weissman)首創,他們最近都獲得了2021年拉斯克獎(Lasker Award),這是美國最高生物醫學研究獎。不過,即使在2019年,主流mRNA疫苗也被認為至少需要5年時間。大流行使這一醫學領域進展快了五年。卡耐基梅隆大學(Carnegie Mellon University)化學工程和生物醫學工程副教授、韋斯曼和卡里科的重要合作者凱瑟琳·懷特黑德(Kathryn Whitehead)承認,「在mRNA療法領域,沒有多少人能想象出在這種緊急情況下95%的初始有效性。」
但現在,可能性似乎無窮無盡。正如布拉克尼所說,「現在的情況是,好吧,既然它對一種病毒糖蛋白有效,我們還能用它製造什麼其他疫苗呢?除此之外,我們還能做些什麼?」

在羅切斯特大學(University of Rochester),生物系副教授德拉根尼·傅(Dragony Fu)從美國國家科學基金會獲得了快速資助,用於研究RNA蛋白質。傅教授說,如果我們目前看到的是針對新冠病毒的mRNA疫苗1.0,那麼2.0將解決兩類疾病:「一種是病原體,比如非典,還可以將這種技術應用於其他外來入侵者,比如艾滋病毒。早在新型冠狀病毒出現之前,很多公司就已經在研發針對艾滋病毒的mRNA疫苗。」他還提到了病原體營地裏的寨卡病毒、皰疹病毒和瘧疾寄生蟲。
「另一類是自身免疫性疾病,」他說。「這很有趣,因為它幾乎超出了疫苗的嚴格定義。」傅教授說,未來可能會涉及mRNA「治療」,例如減少炎症。他說:「理論上,這開闢了許多可能性。」
俄亥俄州立大學(Ohio State University)藥劑學和藥理學副教授董一洲專門研究小脂肪球,即脂質,這些脂質需要儲存mRNA,並安全地將其輸送到細胞中,而不被我們的身體立即破壞。脂質被稱為「無名英雄」。如果2018年脂質傳遞最終沒有得到完善和批准,2020年就不會有新冠 mRNA疫苗。董教授說,在新冠病毒之前,許多研究著眼於將這種新的脂質輸送技術與mRNA相結合的更廣泛應用,包括遺傳疾病、癌症免疫治療、傳染病和細菌感染。「只要你有抗原並能對蛋白質進行測序,理論上就應該有效。」
由於脂質輸送和mRNA技術的聯合突破,正在開發的疫苗和治療方法包括:Translate Bio公司的囊性纖維化和多發性硬化症的mRNA療法;Gritstone Oncology公司和Gilead Sciences公司的HIV mRNA疫苗;Arcturus Therapeutics公司的囊性纖維化和心臟病療法;以及德國初創公司Ethris與阿斯利康正在開發用於嚴重肺部疾病和哮喘的mRNA療法。

科學界也正在探索解決熱帶病的辦法。在針對寨卡(Zika)病毒和基孔肯雅(Chikungunya)病毒的臨牀mRNA疫苗試驗中,莫德納已接近第二階段。這兩種疾病都被稱為「被忽視的」,之所以這麼說是因為它們影響了世界上最貧窮的人口,而且沒有得到足夠的研究和資助。mRNA疫苗的速度和成本可能會改變這種模式,並標誌著被忽視的熱帶病即將終結。
不過,也許第一個出現在貨架上的新mRNA疫苗針對的是一種更熟悉的敵人——流感。流感病毒每年造成全世界約29萬至65萬人死亡。「我們很有可能在不久的將來看到針對流感的mRNA疫苗,」懷特黑德說。「這些mRNA疫苗已經研發多年,迄今為止的臨牀試驗令人鼓舞。目前有五項針對甲型流感的臨牀試驗,其中一項處於第二階段」。這可能來得正是時候。英國東安格利亞大學(University of East Anglia)健康保護教授、世衛組織顧問保羅·亨特(Paul Hunter)警告,一些國家可能出現流感大流行,導致死亡人數超過新冠。
一些製藥公司也在研究mRNA疫苗和癌症治療方法。「癌細胞通常會有某些表面標記物,這是體內其他細胞所沒有的,」布拉克尼說。「你可以訓練免疫系統識別並殺死這些細胞,就像可以訓練免疫系統識別並殺死病毒一樣。這是相同的想法,只是找出腫瘤細胞表面的蛋白質,並將其用作疫苗。」根據布萊克尼的說法,針對病人研製個體化藥物的想法多年來一直是個誘人前景——這可能是mRNA打開的另一扇大門。理論上,「他們取出腫瘤,對其進行排序,觀察其表面,然後為你製造專門的疫苗」。

如果對癌症、艾滋病毒和熱帶疾病的治療伴隨著mRNA 2.0而來,那麼在mRNA 3.0的基礎上還有什麼呢?現代醫學的一大擔憂是抗生素耐藥性。布萊克尼說:「你可以想象,實際上可以製造出一種針對細菌抗原的疫苗,比如艱難梭菌或一些非常棘手的細菌。」目前還沒有試驗,但《前沿》(Frontiers)等科學期刊已經探討了這一想法。
也有可能在更廣泛的商業健康和福利方面應用。例如,傅教授建議,乳糖不耐症影響著數以億計的亞洲人,包括他自己,以及估計佔全球人口68%的人。有一天可以成為目標:「我失去了分解乳糖的蛋白質。在未來,你可以開發出某種傳遞信息的方式,mRNA將產生分解乳糖的蛋白質……這不會危及生命,但我可以想象這是價值10億美元的產業。」
在俄亥俄州立大學,董一洲甚至成功進行了一項針對膽固醇的老鼠試驗。PCSK9蛋白水平高的人往往膽固醇含量高,容易早期患心臟病。「我們注意到,(對小鼠)進行一次治療後,我們可以將PCSK9蛋白水平降低95%以上。這絶對是非常重要的研究方向。」董教授表示,至少有一家生物技術公司正在計劃利用mRNA抑制PCSK9的臨牀試驗。
所有這些都提出了一個問題:mRNA療法能給我們帶來幾乎超人的免疫力嗎?新冠mRNA疫苗已經導致一些人產生高水平的抗體,能夠一次性中和幾種新冠病毒變體。
也有可能把不同的mRNA疫苗混合成單一的健康加強疫苗,同時抵禦癌症和病毒。雖然目前這只是推測,但傅教授說,「你可以選擇一大堆不同的口味……一種mRNA的雞尾酒,讓不同的蛋白質根據你的特定需求進行選擇。」莫德納和諾瓦瓦克斯(Novavax)都已經在研發新冠病毒和流感病毒的組合疫苗。

但先不要得意的太早,關於mRNA疫苗還有一些問題。我們目前需要定期加強注射,而注射往往會傷害手臂,有時還會產生疲勞的副作用。在寫這篇文章的時候,mRNA疫苗在現實世界中使用還不到一年。在美國,每百萬人接種疫苗中約有2至5人出現過敏反應(儘管沒有死亡):輝瑞疫苗的過敏反應略高,為每百萬人4.7人,而莫德納疫苗的過敏反應為每百萬人2.5人。根據一項分析,儘管數量仍然很低,但這是流感疫苗的11倍。
「我們仍在努力了解抗體反應和細胞反應持續多長時間,」布萊克尼說。「現在有很好的跡象表明,你確實從mRNA疫苗中獲得了非常好的記憶T細胞反應,但由於這些試驗在大多數情況下已經進行了一年半,我們可以了解免疫持續了多長時間。」她還說,大多數人「真的不想每年接種多次疫苗,然後在接種後倒下三天」。
不過,布拉克尼在英屬哥倫比亞大學的實驗室正在研究一個答案:saRNA,或自擴增mRNA。它與正常的mRNA有相同的結構,不過一旦進入細胞,它可以自我複製。「這非常有利,因為你可以使用更低的劑量,通常大約是mRNA的100倍,」布拉克尼說。這意味著成本更低,手臂疼痛更少。在龜兔賽跑中,mRNA疫苗已經能夠戰勝新冠病毒,但saRNA可能最終勝出——實際上,它剛剛從阿斯利康公司獲得了1.95億美元的支持(這與本文前面提到的Ethris為其肺部疾病疫苗開發獲得的2950萬美元相比更有優勢)。
與此同時,傅教授、董教授、懷特黑德和布萊克尼繼續駕馭著「RNA復興」的浪潮。無論他們在哪裏,有一件事是肯定的:這再也不會是不為人知的研究領域。尤其是當你像布拉克尼一樣把解說視頻放到TikTok上。她笑著說:「我在那裏的任務是教育人們有關疫苗的知識。我收到大量隨機問題。但也有很多人說,因為你,我和我的伙伴才接種了疫苗。真的很有影響力。」
請訪問 BBC Future 閲讀 英文原文。
本網頁內容為BBC所提供, 內容只供參考, 用戶不得複製或轉發本網頁之內容或商標或作其它用途,並且不會獲得本網頁內容或商標的知識產權。

10/04/2024 10:44AM

09/04/2024 05:00PM

09/04/2024 05:00PM